
Barış Genç et al. Clin Transl Med. 2021 febrero.
Antecedentes: Las neuronas motoras superiores (UMN) son un componente clave del circuito de las neuronas motoras. Su degeneración es un sello distintivo de enfermedades como la paraplejia espástica hereditaria (HSP), la esclerosis lateral primaria (PLS) y la esclerosis lateral amiotrófica (ELA). Actualmente no existen ensayos preclínicos que investiguen las respuestas celulares de las UMN al tratamiento compuesto, ni siquiera para enfermedades de las UMN. La base de la vulnerabilidad de las UMN no se comprende completamente y aún no se ha identificado ningún compuesto que mejore la salud de las UMN enfermas:dos obstáculos importantes para desarrollar estrategias de tratamiento efectivas.
Métodos: Los nuevos modelos informadores de UMN, en los que las UMN que están enfermas debido a la toxicidad de la proteína superóxido dismutasa (mSOD1) mal plegada y la patología TDP-43 están marcadas con expresión de eGFP, permiten una evaluación directa de la respuesta de la UMN al tratamiento compuesto. La microscopía electrónica revela aspectos muy precisos del retículo endoplasmático (RE) y del daño mitocondrial. La administración de NU-9, un compuesto identificado inicialmente en función de su capacidad para reducir la toxicidad de mSOD1, tiene un profundo impacto en la mejora de la salud y la estabilidad de las UMN, como se identifica mediante análisis celulares y ultraestructurales detallados.
Resultados: Los problemas con las mitocondrias y el RE se conservan en las UMN enfermas entre diferentes especies. NU-9 tiene propiedades farmacocinéticas similares a las de un fármaco. Carece de toxicidad y atraviesa la barrera hematoencefálica. NU-9 mejora la integridad estructural de las mitocondrias y el RE, reduce los niveles de mSOD1, estabiliza las dendritas apicales de UMN en degeneración, mejora el comportamiento motor medido mediante la prueba del alambre colgante y elimina la degeneración continua de UMN que enferman tanto debido a la toxicidad de mSOD1 como a la patología de TDP-43, dos causas generales distintas e importantes de la degeneración de las neuronas motoras.
Conclusiones: Los enfoques de descubrimiento de fármacos centrados en mecanismos y basados en células no solo abordaron defectos celulares clave responsables de la pérdida de UMN, sino que también identificaron NU-9, el primer compuesto que mejora la salud de las UMN enfermas, neuronas que degeneran en pacientes con ELA, HSP, PLS y ELA/FTLD.
Palabras clave: ELA; HSP; NU-9; por favor; patología TDP-43; mSOD1; neuronas motoras superiores.
© 2021 Los Autores. Medicina clínica y traslacional publicado por John Wiley &Sons Australia, Ltd en nombre del Instituto de Bioinformática Clínica de Shanghai.
Descargo de responsabilidad de PubMed
Los autores declaran que no existe ningún conflicto de intereses.
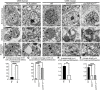 FIGURA 1
FIGURA 1 Las neuronas motoras superiores (UMN) muestran defectos ultraestructurales en pacientes con esclerosis lateral amiotrófica (ELA) y en modelos de ratón que están enfermos debido a diferentes causas subyacentes. (A) Imagen representativa de microscopía electrónica (EM) de UMN de control normal aparece intacta, mientras que (B) UMN de un paciente con ELA muestra defectos citoarquitectónicos. (C) Imagen EM de UMN de ratón WT. (D) Imagen EM representativa de UMN de hSOD1G93A y (E) ratón prpTDP-43A315T que muestra una desintegración ultraestructural masiva. (F) Las mitocondrias en un control normal que muestran membranas mitocondriales internas intactas (flechas), a diferencia de (G) mitocondrias en pacientes con ELA que muestran la desintegración de la membrana mitocondrial interna (puntas de flecha). (H) Las mitocondrias en ratones WT parecen estar estructuralmente intactas con membranas mitocondriales internas y externas distintas (flecha), mientras que (I) las mitocondrias en UMN en un ratón hSOD1G93A y (J) prpTDP-43A315T muestran una desintegración severa de las membranas mitocondriales internas (puntas de flecha). (K) Las micrografías electrónicas del retículo endoplásmico (ER) de la UMN en un control normal muestran cisternas largas correctamente apiladas (flechas), pero (L) el ER en un paciente con ELA muestra distensión y abombamiento de las cisternas del ER (puntas de flecha). De manera similar, (M) ER en un ratón WT (flechas) parece estructuralmente intacto en contraste con (N) ER en UMN de hSOD1G93A y (O) ratón prpTDP-43A315T que muestra cisternas de ER rotas, cortas y desintegradas (puntas de flecha). (P) Cuantificación del porcentaje promedio de RE con defectos citoarquitectónicos/UMN en pacientes con ELA. ****p < .0001, prueba t de Student. (Q) Cuantificación del porcentaje promedio de ER con defectos citoarquitectónicos/UMN en hSOD1G93A. ****p < .0001, y ratones prpTDP-43A315T. ****p < .0001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. (R) Cuantificación de la longitud promedio de las cisternas del RE/UMN en pacientes con ELA. **p < .001, prueba t de Student. (S) Cuantificación de la longitud promedio de las cisternas del RE/UMN en ratones hSOD1G93A **** p < .0001 y prpTDP-43A315T. ****p < .0001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. Barras de escala:A – E = 2 μm; F–O = 200 nm
 FIGURA 2
FIGURA 2 El tratamiento con NU-9 mejora la integridad ultraestructural tanto de las mitocondrias como del retículo endoplásmico (ER) de las neuronas motoras superiores (NMS) que enferman por la toxicidad de SOD1 mutante. (A) Progresión desde el impacto hasta llegar a NU-9 con estructura química de NU-9. (B) Diseño experimental para estudios in vivo. (C – F) Imágenes representativas de microscopía electrónica (EM) de UMN en la corteza motora de ratones WT-UeGFP tratados con vehículo en P120. Las flechas apuntan a las mitocondrias con la membrana interna intacta y al RE con las cisternas intactas. Barras de escala, C:2 µm; D–F:200 nm. (G – J) Imágenes EM representativas de UMN en la corteza motora de ratones hSOD1G93A‐UeGFP tratados con vehículo en P120. (G) El citoplasma carece en su mayor parte de orgánulos clave importantes y (H) hay numerosos agregados densos en electrones (puntas de flecha) y gotas grandes. (I) Son evidentes las mitocondrias que perdieron la integridad de su membrana interna (punta de flecha) o tienen daño estructural general, y (J) piezas fragmentadas del RE (puntas de flecha). Barras de escala, G:2 µm; H-J:200 nm. (K–N) Imágenes EM representativas de UMN en la corteza motora de ratones hSOD1G93A‐UeGFP tratados con 100 mg/kg/día de NU‐9. (K) Mejora general del citoplasma con presencia de numerosos orgánulos. (L) Las mitocondrias parecen estar sanas (flechas) y el citoplasma carece de gotitas y agregados densos importantes. (M) Se restaura la integridad de la membrana mitocondrial interna y la estructura de las crestas (flechas), y (N) las cisternas del RE (flechas) se organizan en la estructura adecuada sin ninguna fragmentación. Barras de escala, I:2 µm; L–N:200 nm. (O) Cuantificación del número total de mitocondrias/UMN en ratones hSOD1G93A‐UeGFP con tratamiento con NU‐9. **p < .006, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. (P) Cuantificación del porcentaje de mitocondrias/UMN sanas en ratones hSOD1G93A‐UeGFP con tratamiento con NU‐9. ****p < .0001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. (Q) Cuantificación del número de cisternas del RE/UMN en ratones hSOD1G93A‐UeGFP con tratamiento con NU‐9. *p < .016, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. (R) Cuantificación de la longitud promedio de las cisternas del RE/UMN en ratones hSOD1G93A-UeGFP con tratamiento con NU-9. **p < .002, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey
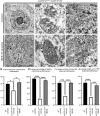 FIGURA 3
FIGURA 3 El tratamiento con NU-9 reduce los niveles de SOD1 mal plegado en las neuronas motoras superiores (UMN) de ratones hSOD1G93A-UeGFP. (A) Imágenes representativas de UMN y tinción de anticuerpos B8H10 que reconoce la proteína SOD1 mal plegada en la corteza motora de ratones WT-UeGFP o (B) hSOD1G93A-UeGFP tratados con vehículo, (C) 20 mg/kg/día NU-9, o (D) 100 mg/kg/día NU-9. Barras de escala, 20 μm; n ≥ 3 réplicas biológicas. (E) Densidad integrada promedio de fluorescencia de SOD1 mal plegada en UMN en la corteza motora de ratones WT-UeGFP o hSOD1G93A-UeGFP tratados con vehículo, 20 mg/kg/día NU-9 o 100 mg/kg/día NU-9; media, SEM y puntos de datos individuales mostrados para n ≥ 3 réplicas biológicas. **p < .01, ****p < .0001, ANOVA unidireccional seguido de la prueba post hoc de comparación múltiple de Tukey
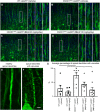 FIGURA 4
FIGURA 4 El tratamiento con NU-9 mejora la integridad citoarquitectónica de las dendritas apicales en desintegración de las neuronas motoras superiores (UMN) que enferman por la toxicidad de SOD1 mal plegada. (A) Imágenes representativas de dendritas apicales UMN en la corteza motora de ratones WT-UeGFP o (B) hSOD1G93A-UeGFP tratados con vehículo, (C) 20 mg/kg/día NU-9, o (D) 100 mg/kg/día NU-9. Las áreas encuadradas se amplían hacia la derecha y se proporcionan ejemplos adicionales. Barras de escala:50 µm (magnitud baja), 10 µm (inserción de magnitud alta); n ≥ 6 réplicas biológicas. (E) Imagen representativa de una dendrita apical sana, intacta y (F) enferma y en desintegración. Barras de escala:5 µm. (G) Porcentaje promedio de dendritas apicales UMN con vacuolas por sección en la corteza motora; media, SEM y puntos de datos individuales mostrados para n ≥ 6 réplicas biológicas. *p < .05, **p < .01, ANOVA unidireccional seguido de la prueba post hoc de comparación múltiple de Tukey
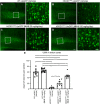 FIGURA 5
FIGURA 5 El tratamiento con NU-9 reduce la degeneración de la neurona motora superior (NMS) de las NMS enfermas como resultado de la toxicidad de SOD1 mal plegada in vivo. (A – D) Imágenes representativas de UMN en la corteza motora de ratones WT-UeGFP o hSOD1G93A-UeGFP tratados con vehículo, 20 mg/kg/día NU-9 o 100 mg/kg/día NU-9. Barras de escala:50 µm; n ≥ 5 réplicas biológicas. (E) Número promedio de UMN por sección en la corteza motora; media, SEM y puntos de datos individuales mostrados para n ≥ 5 réplicas biológicas. *p < .05, ***p < .001, ****p < .0001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey
 FIGURA 6
FIGURA 6 El tratamiento con NU-9 mejora la integridad ultraestructural tanto de las mitocondrias como del retículo endoplasmático (ER) de las neuronas motoras superiores (NMS) que enferman debido a la patología TDP-43. Los defectos mitocondriales y del RE en las UMN de ratones prpTDP-43A315T-UeGFP se publicaron previamente. (A – C) Imágenes representativas de microscopía electrónica de UMN de ratones prpTDP-43A315T-UeGFP no tratados. (A) Soma UMN, con pocos orgánulos intactos. (B) Las mitocondrias pierden la integridad de su membrana interna (puntas de flecha) y (C) las cisternas del RE se desintegran y se rompen (puntas de flecha). (D – F) Imágenes representativas de microscopía electrónica de UMN de ratones prpTDP-43A315T-UeGFP tratados con 100 mg/kg/día de NU-9. (D) Se evidencia una mejora general en la citoarquitectura con una membrana nuclear adecuada, la presencia de numerosos orgánulos sanos y la falta de agregados densos en electrones. (E) Las mitocondrias parecen sanas con membrana interna y crestas mejoradas (flecha) (F), y cisternas del RE dispuestas en una estructura adecuada con ribosomas adheridos (flechas). Barras de escala:A,D:2 µm; B,C,E,F:200 nm. (G) Cuantificación del número total de mitocondrias/UMN en ratones prpTDP-43A315T-UeGFP con tratamiento con 100 mg/kg/día de NU-9; *p < .03. (H) Cuantificación del porcentaje de mitocondrias/UMN sanas en ratones prpTDP‐43A315T‐UeGFP con tratamiento con 100 mg/kg/día de NU‐9; ****p< .0001. (I) Cuantificación del número de cisternas del RE/UMN en ratones prpTDP‐43A315T‐UeGFP con tratamiento con 100 mg/kg/día de NU‐9; ***p < .0003. (J) Cuantificación de la longitud promedio de las cisternas del RE/UMN en ratones prpTDP-43A315T-UeGFP con tratamiento con 100 mg/kg/día de NU-9; ****p< .0001. Para los análisis estadísticos se utilizó ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey.
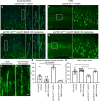 FIGURA 7
FIGURA 7 El tratamiento con NU-9 mejora la integridad citoarquitectónica de las dendritas apicales en desintegración y elimina la degeneración progresiva de las neuronas motoras superiores (NMS) que enferman debido a la patología TDP-43. (A) Imágenes representativas de dendritas apicales UMN en la corteza motora de ratones prpTDP-43A315T-UeGFP no tratados y (B) ratones prpTDP-43A315T-UeGFP tratados con 100 mg/kg/día de NU-9. El área del recuadro se amplía hacia la derecha con ejemplos representativos adicionales. Barras de escala:50 µm (magnitud baja), 10 µm (inserción de magnitud alta); n ≥ 3 réplicas biológicas. (C) Imagen representativa de una dendrita apical sana, intacta y (D) enferma y en desintegración. Barras de escala:5 µm. (E) Porcentaje promedio de dendritas apicales con vacuolas por área de sección en la corteza motora; media, SEM y puntos de datos individuales mostrados para n ≥ 3 réplicas biológicas. **p < .01, ***p < .001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. (F) Imágenes representativas de UMN en la corteza motora de ratones prpTDP-43A315T-UeGFP no tratados y (G) prpTDP-43A315T tratados con 100 mg/kg/día de NU-9. Barras de escala:50 µm; n ≥ 3 réplicas biológicas. (H) Número promedio de UMN por área de sección en la corteza motora; media, SEM y puntos de datos individuales mostrados para n ≥ 3 réplicas biológicas. *p < .05, **p < .01, ***p < .001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey
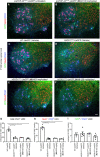 FIGURA 8
FIGURA 8 El tratamiento con NU-9 no mejora la degeneración de la neurona motora inferior (NMI) resultante de la toxicidad de SOD1 mal plegada in vivo. (A y B) Imágenes representativas de NMI en la médula espinal lumbar de ratones prpTDP-43A315T-UeGFP no tratados o tratados con 100 mg/kg/día NU-9. Barra de escala:50 µm; n ≥ 3 réplicas biológicas. (C – F) Imágenes representativas de LMN en la médula espinal lumbar de ratones WT-UeGFP o hSOD1G93A-UeGFP tratados con vehículo, 20 mg/kg/día NU-9 o 100 mg/kg/día NU-9. Barra de escala:50 µm; n = 5 réplicas biológicas. (G) Número promedio de ChAT+ LMN por sección en la médula espinal lumbar; media, SEM y puntos de datos individuales mostrados para n = 5 réplicas biológicas. ****p < .0001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. (H) Número promedio de LMN NeuN+/ChAT+ (vulnerables a la degeneración) por sección en la médula espinal lumbar; media, SEM y puntos de datos individuales mostrados para n = 5 réplicas biológicas. ****p < .0001, ANOVA unidireccional seguido de la prueba de comparación múltiple post hoc de Tukey. (I) Número promedio de LMN GFP+/ChAT+ (resistentes a la degeneración) por sección en la médula espinal lumbar; puntos de datos medios, SEM y individuales mostrados para n = 5 réplicas biológicas
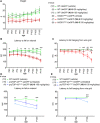 FIGURA 9
FIGURA 9 Datos de comportamiento de ratones WT‐UeGFP, hSOD1G93A‐UeGFP y prpTDP‐43A315T‐UeGFP con o sin tratamiento con NU‐9. Se analizaron ratones WT-UeGFP y hSOD1G93A-UeGFP cada 7 días entre el día posnatal (P)60 y P120; Se probaron ratones prpTDP‐43A315T‐UeGFP en P60, P90 y P120. (A) Peso de los ratones en gramos. Se muestra la media y el SEM para n ≥ 5 ratones por grupo. WT‐UeGFP (vehículo) versus hSOD1G93A‐UeGFP (vehículo); #p < .05, ANOVA de dos factores con la prueba de comparación múltiple de Tukey. (B) Latencia para caer al acelerar el rotarod en segundos. Se muestra la media y el SEM para n ≥ 5 ratones por grupo. WT‐UeGFP (vehículo) versus hSOD1G93A‐UeGFP (vehículo). #p < .05, ##p < .01, ###p < .001, ####p < .0001, ANOVA de dos vías con la prueba de comparación múltiple de Tukey. (C) Latencia para caer colgado boca abajo de una rejilla de alambre en segundos. Se muestra la media y el SEM para n ≥ 5 ratones por grupo. WT‐UeGFP (vehículo) versus hSOD1G93A‐UeGFP (vehículo). #p < .05, ###p < .001, ####p < .0001; hSOD1G93A‐UeGFP (vehículo) versus hSOD1G93A‐UeGFP (NU‐9 100 mg/kg/día). *p < .05, ***p < .001, ****p < .0001, ANOVA de dos factores con la prueba de comparación múltiple de Tukey. (D) Latencia para caer al acelerar el rotarod en segundos. Se muestra la media y el SEM para n ≥ 4 ratones por grupo. WT‐UeGFP (vehículo) versus prpTDP‐43A315T‐UeGFP (vehículo). ##p < .01, ####p < .0001, Análisis de efectos mixtos con la prueba de comparación múltiple de Tukey. (E) Latencia para caer colgado boca abajo de una rejilla de alambre en segundos. Se muestra la media y el SEM para n ≥ 3 ratones por grupo. WT‐UeGFP (vehículo) versus prpTDP‐43A315T‐UeGFP (vehículo), ####p < .0001; prpTDP‐43A315T‐UeGFP (sin tratamiento) versus prpTDP‐43A315T‐UeGFP (NU‐9 100 mg/kg/día), ****p < .0001, análisis de efectos mixtos con la prueba de comparación múltiple de Tukey